
钍基核裂变能全国重点实验室 |
|||
|
-钍基核能物理中心-
|
|||
熔盐机械工程技术部 |
|||
仪控工程技术部 |
|||
熔盐化学工程技术部 |
|||
|
-核能综合利用研究中心-
|
|||
材料研究部 |
|||
钍铀循环化学部 |
|||
应用化学技术部 |
|||
氚科学与工程技术部 |
|||
核与辐射安全技术部 |
|||
应用加速器技术部 |
|||
反应堆运行技术部 |
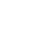



2015年8月26日,清华大学生命科学学院柴继杰教授研究组、中科院遗传与发育研究所杨维才研究员研究组合作在《Nature》在线发表《植物肽激素phytosulfokine受体的别构激活机制》(Allosteric receptor activation by the plant peptide hormone phytosulfokine)研究论文,揭示了植物重要肽类激素phytosulfokine (PSK)的识别和受体激活分子机理。
植物肽类激素同植物经典激素一样,对植物体的生长发育等生理活动具有重要的调控作用。PSK是较早被发现和研究的一种含两个酪氨酸磺化修饰的五肽激素,在植物的生长发育、抗逆和先天免疫等方面有广泛调控作用。PSK发挥活性是通过与细胞膜上的受体激酶PSKR结合来发挥功能,但PSK被受体PSKR识别的分子机理以及后续的受体激活机制还需要阐明。
柴继杰研究组利用上海光源生物大分子晶体学线站(BL17U1)解析了PSKR胞外区结合PSK的复合物结构,阐明了PSKR胞外区通过其岛区来识别PSK的分子机理。深入的结构分析提示SERK家族成员可能作为共受体参与PSKR的受体激活,体外生化实验初步证实了这一假设,同时通过与中科院遗传与发育研究所杨维才研究员研究组合作,利用植物体内生化和遗传学的方法最终证明了这一假设。这也是通过结构生物学提示找到PSK信号转导通路上的新成份。通过解析和对比分析PSKR-PSK-SERK三元复合物结构和单独的PSKR结构,揭示了PSK通过诱导原本无序的受体PSKR岛区产生与共受体SERK结合的新界面从而别构激活受体PSKR的新机制。
PSK-PSKRLRR-SERKLRR激活复合物是第一个植物肽类激素的激活复合物结构,为其他植物肽类激素的研究提供了思路,进一步推广了植物受体激酶异元二聚化的活化模式和SERK家族的信号枢纽功能。从结构角度首次揭示配体通过别构诱导受体构象变化来介导受体与共受体互作的活化模式,区别于BRI1和FLS2通过配体的“胶联”作用结合共受体的这一类似于植物经典激素受体活化的“分子胶”模式。基于PSK受体结构的PSK类似物的研发可用作提高作物产量的生长添加剂,具有重要的实际应用意义。

图示(A)PSK-PSKR识别复合物结构;(B)PSKR-SERK在植物体水平的互作;(C)PSK-PSKR-SERK激活复合物结构;(D)单独的PSKR和结合PSK的PSKR结构比较。
另外,清华大学颜宁教授研究组和杨茂君教授研究组近期分别在《科学》和《自然》发表了关于MvINS蛋白和Piezo1离子通道的研究论文。
清华大学颜宁研究组7月10日在《科学》(Science)发表题为《分枝杆菌Insig同源蛋白晶体结构揭示Insig蛋白感受固醇的分子机制》(Crystal structure of a mycobacterial Insig homolog provides insight into how these sensors monitor sterol levels)的研究论文,报道了一类分支杆菌中Insig同源蛋白MvINS的高分辨率晶体结构,并通过大量生化分析揭示了人源Insig蛋白感受调控细胞内固醇类分子水平的生化机制。相关研究过程中利用上海光源生物大分子晶体学线站(BL17U1)解析了MvINS突变体的晶体结构。
清华大学杨茂君研究组、肖百龙研究组和高宁研究组合作9月21日在《Nature》杂志上以长文形式在线发表了题为《哺乳动物机械敏感Piezo1离子通道的结构》(Architecture of the Mammalian Mechanosensitive Piezo1 Channel)的研究论文,首次报道了哺乳动物机械力敏感Pieze离子通道的冷冻电镜结构,为理解其离子流通、机械力感受及门控机制提供了重要线索。相关研究过程中利用上海光源生物大分子晶体学线站(BL17U1)解析了CED结构域的母体晶体结构。CED在晶体结构中形成同源三聚体,将其与Piezo1离子通道电镜密度拟合,发现CED三聚体形成了Piezo1离子通道中的“cap”区域,进一步支持了Piezo1离子通道是同源三聚体的结论。(生命科学研究部 供稿)