
钍基核裂变能全国重点实验室 |
|||
|
-钍基核能物理中心-
|
|||
熔盐机械工程技术部 |
|||
仪控工程技术部 |
|||
熔盐化学工程技术部 |
|||
|
-核能综合利用研究中心-
|
|||
材料研究部 |
|||
钍铀循环化学部 |
|||
应用化学技术部 |
|||
氚科学与工程技术部 |
|||
核与辐射安全技术部 |
|||
应用加速器技术部 |
|||
反应堆运行技术部 |
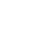



近期,中国科学院上海应用物理研究所左小磊研究员等应邀在《自然-实验方法》撰写了精确自组装电化学传感方面的实验方法论文(Nature Protocols 2016, 11, 1244),系统阐述了精确自组装DNA四面体纳米结构的设计、制备、表征及其在电极界面上的组装过程,并建立了多分子水平检测生物靶标的生物传感平台。
癌症的发生发展过程关系到DNA、RNA、蛋白质和代谢小分子等多个分子水平的变化。因而,单一肿瘤标志物的检测难以满足癌症精准检测的需求。上海应用物理研究所樊春海团队基于DNA纳米技术发展了精确自组装的DNA四面体纳米结构,在国际上率先提出利用三维DNA纳米结构进行界面调控的电化学生物传感策略(Adv. Mater. 2010, 22, 4754)。左小磊与樊春海等密切合作,充分利用DNA纳米结构精确可调的特点,在金电极上构筑了纳米尺度精确可控的自组装界面(Angew. Chem. Int. Ed. 2015, 54, 2151;Adv. Mater. 2016, doi: 10.1002/adma.201506407),并进一步发展了针对蛋白质、核酸(DNA/RNA)、小分子等不同分子水平靶标的高灵敏检测方法(Anal.Chem. 2014, 86, 2124; Anal.Chem. 2014, 86, 7337; Anal.Chem. 2014, 86, 7843)。基于这一精确自组装策略发展的通用生物检测平台为实现多分子水平肿瘤标志物的联合奠定了基础,为实现癌症早期精准检测提供了强有力的工具。Nature Protocols审稿人评价这一工作:“迈出了非常重要的一步,在技术创新与实际应用之间构筑起一道桥梁”。(物理生物学研究室 供稿)
