
钍基核裂变能全国重点实验室 |
|||
|
-钍基核能物理中心-
|
|||
熔盐机械工程技术部 |
|||
仪控工程技术部 |
|||
熔盐化学工程技术部 |
|||
|
-核能综合利用研究中心-
|
|||
材料研究部 |
|||
钍铀循环化学部 |
|||
应用化学技术部 |
|||
氚科学与工程技术部 |
|||
核与辐射安全技术部 |
|||
应用加速器技术部 |
|||
反应堆运行技术部 |
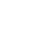



2016年12月6日,清华大学生命学院、结构生物学高精尖创新中心陈柱成研究组在《自然》(Nature)发表题为“Structure and regulation of the chromatin remodeller ISWI”的研究论文。该工作利用上海光源生物大分子晶体学线站(BL17U1)解析了嗜热酵母的ISWI蛋白以及ISWI蛋白与组蛋白H4复合物的原子分辨率结构;结合相应的生化实验,揭示了ISWI蛋白的自抑制、被底物识别与激活以及感知接头DNA的长度,发挥染色质组装功能的分子机理。
染色质是真核生物的生命蓝图。染色质重塑蛋白利用ATP水解的能量,改变染色质结构,参与生命蓝图的绘制和重绘。ISWI是多个染色质重塑复合物的催化亚基。ISWI驱动核小体在基因组DNA上滑动,调控基因转录、异染色质形成、X-染色体失活以及其它重要的染色质活动。ISWI蛋白的催化核心是一个自主的染色质重塑分子机器,其运作受严格的调控。ISWI活性受到AutoN结构域和NegC结构域的抑制作用,确保ISWI分子机器在没有结合底物时不会消耗ATP的能量。这些抑制作用分别被底物核小体的组蛋白H4尾巴和接头DNA拮抗。然而,组蛋白H4的乙酰化修饰削弱其对ISWI激活,这些多层次的调控作用确保细胞形成正确的高级染色质结构,保证正常的生命活动。
该研究揭示了ISWI的AutoN包含两个抑制元件,均与core2结合,使得ISWI处于抑制状态。组蛋白H4尾巴与core2的一个负电荷表面结合,与其中一个AutoN抑制元件有竞争关系,从而解析了H4激活ISWI以及乙酰化作用细调ISWI活性的分子机理。进一步生化研究表明ISWI蛋白的NegC与core2存在相互作用,这种相互作用是ISWI蛋白通过HSS结构域感知接头DNA长度、发挥染色质组装功能的分子基础。(生命科学部 供稿)
图:嗜热酵母ISWI蛋白的晶体结构
原文链接:http://www.nature.com/nature/journal/vaop/ncurrent/full/nature20590.html